آگروباکتریوم (Agrobacterium)
آگروباکتریوم نوعی باکتری گرم منفی است که توسطH. J. Conn شناسایی شد. آگروباکتریوم تومیفاسینس (Agrobacteriu tumefaciens) گونه ای از این جنس است که مورد مطالعه بیشتری قرار گرفته است. این باکتری توانایی انتقال افقی ژن های خود به گیاه را داشته و به دلیل انتقال این ژنها باعث ایجاد گال یا تومور در گیاهان می شود. به دلیل این توانایی ( انتقال DNA بین خود و گیاهان) به یک ابزار مهم در مهندسی ژنتیک تبدیل شده است. در مطالعات تاکسونومی اخیر، گونههای آگروباکتریوم در جنس های جدیدی مانند Ahrensia، Pseudorhodobacter، Ruegeria و Stappia طبقهبندی شده اند(۱ و ۲) اما اغلب آنها در دسته Rhizobium قرار دارند(۳ و ۴ و ۵).
آگروباکتریوم پاتوژن گیاهی:
آگروباکتریوم تومیفاسینس باعث بیماری گال تاجی(crown-gall disease) در گیاهان میشود. این بیماری با رشد تومور مانند و یا گال بر روی گیاه آلوده (اغلب در محل اتصال بین ریشه و ساقه) شناخته میشود. تومورها به علت انتقال یک قطعه DNA (T-DNA) ایجاد می شود. این قطعه T-DNA از پلاسمید القاکننده ی تومور باکتریایی (bacterial tumor-inducing (Ti) plasmid) و با مکانیسم هم یوغی انتقال می یابد.
پلاسمید T-DNA به صورت نیمه تصادفی به ژنوم سلول میزبان وارد میشود (6) و بیان ژن های ایجاد کننده تومور موجود در T-DNA، باعث شکل گیری گال میگردد.
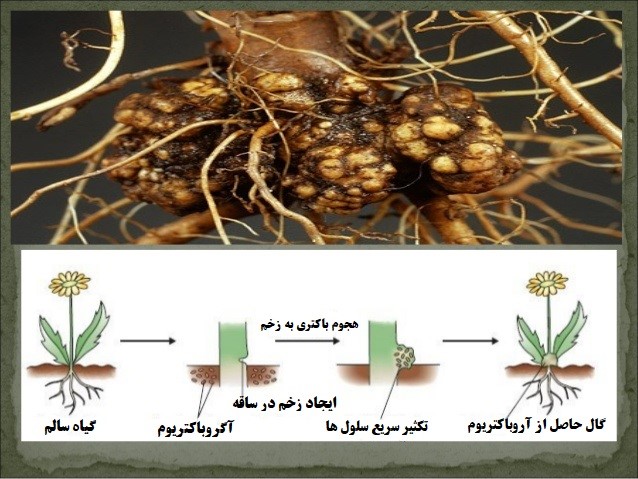
گال های القا شده توسط باکتری آگروباکتریوم در گیاه
آگروباکتریوم و انسان:
اگر چه آگروباکتریوم به طور کلی به عنوان یک عفونت گیاهی محسوب می شود، اما میتواند مسئول عفونت های فرصت طلب در انسان نیز باشد (۷ و ۸). این عفونت زمانی در انسان ایجاد می شود که سیستم ایمنی ضعیف باشد. این باکتری به عنوان یک عامل بیماریزای مهم در افراد سالم گزارش نشده است.
کاربرد آگروباکتریوم در زیست فناوری:
توانایی آگروباکتریوم در انتقال ژن به گیاهان و قارچ ها، باعث شده تا این باکتری در زیست فناوری و به طور خاص در مهندسی ژنتیک به منظور بهبود گیاهان استفاده شود. میتوان از یک پلاسمید تغییر یافته Ti یا Ri برای انتقال ژن مورد نظر استفاده کرد. ژنهای القا کنندهی تومور از پلاسمید حذف شده و تنها قطعات ضروری T-DNA که شامل دو تکرار 25 جفت بازی است باقی میماند که حداقل یکی از آنها برای انتقال به گیاه مورد نیاز است (۹ و ۱۰). ژنی که قرار است به گیاه وارد شود به درون یک وکتور انتقالی گیاهی فرستاده می شود. این وکتور شامل ناحیهT-DNA ی پلاسمید ذکر شده به همراه یک نشانگر انتخابی (مانند مقاومت به آنتی بیوتیک) است. نشانگر انتخابی به منظور شناسایی گیاهانی که انتقال در آنها با موفقیت انجام شده، مورد استفاده قرار میگیرد. گیاهان پس انتقال بر روی محیط های حاوی آنتی بیوتیک رشد داده میشوند تا آنهایی که T-DNA را به درون ژنوم خود راه ندادهاند، بمیرند. یک روش جایگزین، آگرواینفیلتراسیون (agroinfiltration) است(۱۱ و ۱۲).
مکانیسم انتقال ژن بین آگروباکتریوم و گیاهان توسط مارک ون مونتاگ و جوزف شل در دانشگاه گنت (بلژیک) کشف شد. این کشف منجر به توسعه روش هایی برای تغییر آگروباکتریوم به یک سیستم انتقالی کارآمد برای مهندسی ژن در گیاهان گردید (۹ و ۱۰).
آگروباکتریوم همه گونههای گیاهی را آلوده نمی کند، اما چندین روش موثر دیگر برای انتقال ژن به گیاه وجود دارد که از آن جمله می توان تفنگ ژنی را نام برد.
آگروباکتریوم به عنوان وکتور و یا حامل مواد ژنتیکی برای انتقال به سویا، پنبه، ذرت، چغندر قند، یونجه گندم، روغن کلزا (کانولا) و برنج مورد استفاده قرار گرفته است (13).
ژنوم آگروباکتریوم :
توالییابی ژنوم گونههای مختلفی از باکتری آگروباکتریوم، مطالعه سیر تکامل این موجود را امکان پذیر کرده است و اطلاعاتی را در رابطه با ژن ها و سیستم های درگیر در بیماریزایی (pathogenesis)، کنترل های زیستی و همزیستی (symbiosis) در این باکتری را فراهم کرده است. یک یافتهی مهم این احتمال را نشان میدهد که پلاسمیدها منشا کروموزوم های در حال شکل گیری در بسیاری از این باکتری ها هستند. یافته های دیگر نشان میدهد که ساختارهای کروموزومی متنوع در این گروه، آنها را قادر به زندگی به دو شیوه همزیستی و انگلی کرده است. شناخت بیشتر توالی ژنوم گونههای باکتری آگروباکتریوم باعث افزایش درک عملکرد و تاریخچه تکاملی این گروه از میکروب های گیاهی میشود (14).

انتقال ژن با استفاده از آگروباکتریوم، سلولهای آلوده شده شروع به تشکیل پینه در کنار قطعات گیاه می کنند
منابع:
- Uchino, Yoshihito; Yokota, Akira; Sugiyama, Junta (1997). “Phylogenetic position of the marine subdivision of Agrobacterium species based on 16S rRNA sequence analysis”. The Journal of General and Applied Microbiology. 43 (4): 243–247. doi:2323/jgam.43.243. PMID12501326.
- Uchino, Yoshihito; Hirata, Aiko; Yokota, Akira; Sugiyama, Junta (1998). “Reclassification of marine Agrobacterium species: Proposals of Stappia stellulata gen. nov., comb. Nov., Stappia aggregata sp. nov., nom. Rev., Ruegeria atlantica gen. nov., comb. Nov., Ruegeria gelatinovora comb. Nov., Ruegeria algicola comb. Nov., and Ahrensia kieliense gen. nov., sp. nov., nom. Rev”. The Journal of General and Applied Microbiology. 44 (3): 201–210. doi:2323/jgam.44.201. PMID12501429.
- Young, J. M.; Kuykendall, L. D.; Martínez-Romero, E; Kerr, A; Sawada, H (2001). “A revision of Rhizobium Frank 1889, with an emended description of the genus, and the inclusion of all species of Agrobacterium Conn 1942 and Allorhizobium undicola de Lajudie et al. 1998 as new combinations: Rhizobium radiobacter, R. rhizogenes, R. rubi, R. undicola, and R. vitis”. Int J Syst Evol Microbiol. 51 (Pt 1): 89–103. doi:1099/00207713-51-1-89. PMID11211278.
- Farrand, S. K.; Van Berkum, P. B.; Oger, P (2003). “Agrobacterium is a definable genus of the family Rhizobiaceae”. International Journal of Systematic and Evolutionary Microbiology. 53 (5): 1681–7. doi:1099/ijs.0.02445-0. PMID13130068.
- Young, J. M.; Kuykendall, L. D.; Martínez-Romero, E; Kerr, A; Sawada, H (2003). “Classification and nomenclature of Agrobacterium and Rhizobium—a reply to Farrand et al. (2003)”. International Journal of Systematic and Evolutionary Microbiology. 53 (5): 1689–95. doi:1099/ijs.0.02762-0. PMID13130069.
- Francis, Kirk E.; Spiker, Steven (2004). “Identification of Arabidopsis thaliana transformants without selection reveals a high occurrence of silenced T-DNA integrations”. The Plant Journal. 41 (3): 464–77. doi:1111/j.1365-313X.2004.02312.x. PMID15659104.
- Hulse, M.; Johnson, S.; Ferrieri, P. (1993). “Agrobacterium Infections in Humans: Experience at One Hospital and Review”. Clinical Infectious Diseases. 16 (1): 112–7. doi:1093/clinids/16.1.112. PMID8448285.
- Dunne Jr, W. M.; Tillman, J; Murray, J. C. (1993). “Recovery of a strain of Agrobacterium radiobacter with a mucoid phenotype from an immunocompromised child with bacteremia”. Journal of clinical microbiology. 31 (9): 2541–3. PMC265809. PMID 8408587.
- Schell, J.; Van Montagu, M. (1977). “The Ti-Plasmid of Agrobacterium Tumefaciens, A Natural Vector for the Introduction of NIF Genes in Plants?”. In Hollaender, Alexander; Burris, R. H.; Day, P. R.; Hardy, R. W. F.; Helinski, D. R.; Lamborg, M. R.; Owens, L.; Valentine, R. C. Genetic Engineering for Nitrogen Fixation. Basic Life Sciences. 9. pp. 159–79. doi:1007/978-1-4684-0880-5_12. ISBN978-1-4684-0882-9. PMID 336023.
- Joos, H; Timmerman, B; Montagu, M. V.; Schell, J (1983). “Genetic analysis of transfer and stabilization of Agrobacterium DNA in plant cells”. The EMBO Journal. 2 (12): 2151–60. PMC555427. PMID16453483.
- Thomson JA. “Genetic Engineering of Plants” (PDF). Biotechnology. Encyclopedia of Life Support Systems. 3. Retrieved 17 July 2016.
- Leuzinger K, Dent M, Hurtado J, Stahnke J, Lai H, Zhou X, Chen Q (2013). “Efficient Agroinfiltration of Plants for High-level Transient Expression of Recombinant Proteins”. Journal of Visualized Experiments. 77 (50521). doi:3791/50521. PMC3846102. PMID23913006.
- The FDA List of Completed Consultations on Bioengineered Foods Archived May 13, 2008, at the Wayback Machine.Setubal, Joao C.; WOod, Derek; Burr, Thomas; Farrand, Stephen K.; Goldman, Barry S.; Goodner, Brad; Otten, Leon; Slater, Steven (2009). “The Genomics of Agrobacterium: Insights into its Pathogenicity, Biocontrol, and Evolution”. In Jackson, Robert W. Plant Pathogenic Bacteria: Genomics and Molecular Biology. Caister Academic Press. pp. 91–112. ISBN978-1-904455-37-۰

